Автор: Михаил Иоелович, профессор, доктор химических наук, Израиль
Введение.
Как известно, целлюлоза это самый распространенный органический природный полимер количество которого в природе оценивается в 1 триллион тонн [1]. Установлено также, что вследствие фотосинтеза масса целлюлозы ежегодно возрастает приблизительно на 100 миллиард тонн, но приблизительно такое же количество этого полимера извлекается из природы вследствие естественного распада и хозяйственной деятельности. Целлюлоза присутствует в клеточных стенках всех наземных растениях и водорослей, входит в состав защитного покрова (туники) ряда морских животных, а также синтезируется некоторыми видами бактерий, например, Gluconacetobacter xylinus. Содержание целлюлозы в различных видах растений составляет: в стеблях травяных растений 30-40%, в древесине 42-50%, в лубяных растениях 60-75%, в хлопковых волокнах 90-92% [2].
Целлюлоза представляет собой линейный, стереорегулярный, полукристаллический полисахарид, макромолекулы которого состоят из звеньев D-глюкопиранозы, имеющих конформацию «кресла», соединенных друг с другом химическими 1,4-β-гликозидными связями по типу «голова-хвост» [3,4].
Целлюлоза является типичным наноструктурированным полимером [5], первичными структурными элементами которого являются элементарные нанофибриллы диаметром от 3-4 (для целлюлозы травянистых растений) до 10-15 нм (для целлюлозы туницина и водорослей). Каждая элементарная нанофибрилла включает упорядоченные нанокристаллиты (КР) и мало упорядоченные некристаллические нанодомены (НД). Трехмерно-упорядоченные КР являются стабильными и недоступными участками надмолекулярной структуры. Кроме того согласно современным представлениям [5], поверхностные слои кристаллитов имеют паракристаллическую структуру (Рис. 1). В отличие от КР, мало упорядоченные НД являются слабыми и доступными участками нанофибрилл. Молекулярные цепи целлюлозы проходят через несколько кристаллитов и некристаллических областей нанофбриллы, связывая их сильными химическими связями.
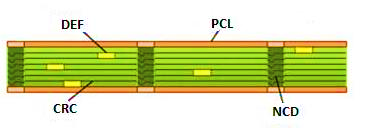
Рис. 1. Модель элементрарной нанофибриллы целлюлозы [5], содержащей кристаллиты (CRC) и некристаллические домены (NCD), а также паракристаллический мономолекулярный поверхностный слой (PCL)
ИЗОЛЯЦИЯ МИКРО- И НАНО РАЗМЕРНЫХ ЧАСТИЦ ЦЕЛЛЮЛОЗЫ
Учитывая, что при кислотном гидролизе целлюлозы кипящими разбавленными кислотами (2-5 М) происходит селективное расщепление доступных мало упорядоченных некристаллических нанодоменов, можно было бы ожидать образования при этом свободных нанокристаллитов. Однако в действительности при таком способе химической обработки целлюлозных волокон вместо нанокристаллитов образуются микрочастицы целлюлозы [6]. Как известно, в клеточных стенках растительных волокон элементарные нанофибриллы целлюлозы разделены аморфными нецеллюлозными компонентами – гемицеллюлозами и лигнином. При выделении целлюлозы из растительного сырья различными методами делигнификации нецеллюлозные компоненты удаляются, что делает возможным прямой контакт элементарных нанофибрилл друг с другом и образование их агрегатов – микрофибрилл (Рис. 2) путем со-кристаллизации поверхностей кристаллитов соседних нанофибрилл, о чем свидетельствует увеличение поперечных размеров кристаллитов после выделения целлюлозы [7-9]. При оптимальных условиях делигнификации может осуществляться удвоение поперечных размеров – двойникование кристаллитов, и образование фибриллярной сетки, связанной прочными локальными кристаллическими контактами.

Рис. 2. Модель микрофибриллы образованной в результате агрегации элементарных нанофибрилл [9]: 1- нанокристаллит; 2- некристаллический домен
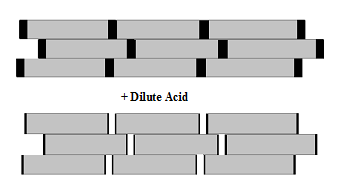
Рис. 3. Схема процесса гидролиза некристаллических доменов целлюлозы разбавленной кислотой с образованием агрегата МКС [10].
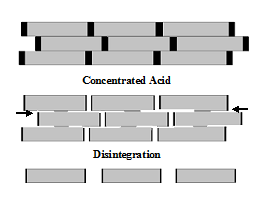
Рис. 4. Схема расщепления НД и межкристаллитных контактов при обработке целлюлозы концентрированными (8-10 М) кислотами [10].
(Стрелки обозначают места межкристаллитной эррозии)
ИЗОЛЯЦИЯ МИКРО- И НАНО ФИБРИЛЛ ЦЕЛЛЮЛОЗЫ
Микрофибриллированную целлюлозу (МФЦ) с высоким выходом (до 90%) получают путем продолжительной механической дезинтеграции разбавленных (0.5-1%) водных дисперсий волокон целлюлозы. Полученная МФЦ представляет собой длинные фибриллярные пучки диаметром до 100 нм [15].
Для облегчения и ускорения процесса фибриллиляции, волокна исходной целлюлозы подвергают предварительной обработке различными методами – путем гидролиза ферментами или разбавленными кислотами, слабого карбоксиметилирования, окисления в присутствии TEMPO-радикалов и другими методами [16-20]. В результате последующей дезинтеграции разбавленных водных дисперсий предобработанных волокон получают нанофибриллированную целлюлозу (НФЦ) — тонкие фибриллярные пучки диаметром 20-40 нм (Рис.5).

Рис. 5. НФЦ полученная дезинтеграцией дисперсии целлюлозных волокон после их кратковременной предобработки целлюлолитическим ферментом [20]
Механические свойства пленок, сформированных из водных дисперсий НФЦ имели модуль Юнга 7-10 ГПа, прочность на разрыв 170-230 МПа, удлинение при разрыве 5-7% и плотность 1.2-1.4 г/см3 [20, 21]. Тонкие пленки, сформированные из разбавленных дисперсий НФЦ были оптически полупрозрачными: прозрачность пленок при длине волны 600 нм составляла около 72% [22].
Водные дисперсии МФЦ и НФЦ характеризуются псевдопластичностью и тиксотропией [23]. Водные дисперсии незаряженных или слабо заряженных НФЦ превращаются в устойчивый гель при относительной низких концентрациях 2-3% [24]. Такой гель имеет динамический модуль порядка 100 кПа и вязкость свыше 50 Па х сек. Повышение заряда НФЦ ухудшает гелеобразующие свойства дисперсий.
ПРОБЛЕМЫ ИСПОЛЬЗОВАНИЯ НАНОЦЕЛЛЮЛОЗЫ
Многочисленные литературные источники (например, [25-30] и др.) отмечают разнообразные потенциальные области применения наночастиц и нанофибриллированной целлюлозы:
- Армирование полимерных композитов
- Наполнение и усиление биоразлагаемых полимерных материалов
- Получение жестких пористых аэрогелей
- Добавка в бумажные композиции для повышения прочности связи между волокнам
- Составная часть покрытий для снижения пористости и увеличения гладкости бумаги
- Составная часть кислородо- и жиронепроницаемых покрытий бумажных упаковочных материалов
- Ультрафильтрация
- Загуститель различных водных систем технического назначения — эмульсий, дисперсий, латексов, клеев, красок, буровых растворов и т.п.
- Водоудерживающая добавка для неорганических связующих
- Диетическая добавка для пищевых продуктов
- Загуститель косметических и лекарственных препаратов
- Нано-эксципиент для таблеток и других фармацевтических препаратов.
- Нано-носитель терапевтически-активных веществ
- Другие области применения
К сожалению, имеются несколько существенных факторов, препятствующих реализации потенциала наноцеллюлозы (НЦ). Во-первых, это высокая себестоимость получения, превышающая $50 за кг сухой НЦ. Это связано с тем, что для изоляции как свободных нанокристаллитов, так и нанофибрилл требуется интенсивная и длительная дезинтеграция разбавленных (0.5-2%) водных дисперсий целлюлозы с использованием гомогенизаторов высокого давления (типа APV-2000), микрофлюидизаторов с высоким напряжением сдвига (типа М-110Р) или ультразвуковых дезинтеграторов. Вследствие этого необходимо затрачивать огромное количество энергии для превращения небольшого количества целлюлозы в нано-форму. В настоящее время пока не создано оборудование, которое бы позволило получать НЦ при высокой концентрации массы с минимальным расходом энергии. В дополнении к этому, для кислотного гидролиза (при получении наночастиц) или для предобработки исходной целлюлозы (при получении НФЦ) требуются повышенные расходы химикатов или использование дорогостоящих ферментов. Конечный результат заключается в том, что расходы энергии и химикатов в расчете на 1кг НЦ становятся настолько большими, что этот нано-продукт не может конкурировать с более дешевыми микроцеллюлозными продуктами (микроволокна, микропорошковая целлюлоза, МКС, микро-производные целлюлозы и др.), которые в настоящее время успешно используются во всех пречисленных выше областях потенциального применения НЦ.
Второй фактор – это отсутствие специфической «ниши», где могла бы использоваться исключительно НЦ, несмотря на ее высокую стоимость.
Третий фактор заключается в том, что использование НЦ в пищевой промышленности, медицине и фармокологии в настоящее время исключено вследствие отсутствия разрешения Минздрава России, FDA США и сооответствующих учерждений других стран. Следует также отметить, что организм человека не имеет ферментов для разложения целлюлозы и поэтому парентеральное применение НЦ исключено.
Заключение: промышленное производство различных типов НЦ пока нецелесообразно вследствие высокой себестоимости и отсутствия специфической «ниши» для их использования.
СПИСОК ЛИТЕРАТУРЫ
- Klemm, D., Heublein, B., Fink H-P., Bohn A. // Angew. Chem. 2005. V. 44. P. 2.
- Young R.A., Rowell R.M. Cellulose: Structure, Modification and Hydrolysis. New York: Wiley, 1986.
- Роговин З.А. Химия целлюлозы. M.: Химия, 1972.
- Гальбрайх Л.С. Целлюлоза и ее производные. М.: Химия, 1996.
- Ioelovich M., Leykin A., Figovsky O. // Bioresources. 2010. V. 5. No 3. P.1393.
- Ioelovich M., Leykin A. // Cellul. Chem. Technol. 2006. V. 40. P. 313.
- Иоелович M.Я. // Химия древесины. Т. 4. С. 27.
- Ioelovich M. // Bioresources. 2008. V. 3. N 4. P. 1403.
- Ioelovich M. // J. Polym. Sci. Ser. A. 2016. V. 58. N 6. P. 925.
- Ioelovich M. // J. SITA. 2016. V.18. N4. P. 72.
- Ioelovich M. Cellulose nanostructured natural polymer. Saarbrücken: LAP, 2014.
- Ioelovich M. // Nanosci. Nanotechn. 2012. V. 2. No 2. P. 9.
- Habibi Y., Lucia, L.A., Rojas O.J. // Chem. Rev. V. 110. P. 3479.
- Ioelovich M. // J. SITA. 2012. V. 14. N 3. P. 91.
- Turbak A.F., Snyder F.W., Sandberg K.R. // J. Appl. Polym. Sci., Appl Polym Symp. 1983. V. 37. P. 815.
- Eichhorn S.J., et al. // Mater. Sci. 2010. V. 45. N 1. P. 1.
- Saito T., Nishiyama T., Putaux J.L., Vignon M., Isogai A. // Biomacromol. 2006. V. 7. P. 1687.
- Janardhnan S., Sain M. // Bioresources. 2006, V.1. N 2. P. 176.
- Janardhnan S., Sain M. // Bioresources. 2011, V.6. N 2. P. 1242.
- Henriksson M. Cellulose Nanofibril Networks and Composites — Preparation, Structure and Properties. Stockholm: KTH, 2008.
- Fukuzumi H. Studies on Structure and Properties of TEMPO-oxidized Cellulose Nanofibril Films. Tokyo: Tokyo University, 2011.
- Dufresne //Mater. Today, 2013. V. 16. N 6. P. 220.
- Lavoine N., Desloges I., Dufresne A., Bras J. // Carbohydrate Polym. V. 90. P. 735.
- Paakko M., Ankerfors M., Kosonen H., et al. // Biomacromol. 2007. V. 8. N 6. P. 1934.
- Hentze H.-P. From Nanocellulose Science towards Applications. Helsinki: VTT, 2010.
- Kalia S., Dufresne A., Cherian B.M., et al. // Int. J. Polym. Sci. 2011. V. 2011. P.1.
- Miao C., Hamad W.Y. // Cellulose. 2013. V. 20. P. 2221.
- Lin N., Dufresne A. // Eur. Polymer J. 2014. V. 59. P. 302.
- Lindström T., Aulin C. // Scand J. Res. 2014. V. 29. P. 345.
- Ioelovich M., Figovsky O., Leykin A. // US Pat. 8268391.
Иллюстрация: Фото: Наноцеллюлоза — ПЕЧАТНИК.com











